質粒制備
雲舟生物平台可滿足基因治療藥物研發(fā)管線全過(guò)程所涉及山刀的載體設計,克隆構建以及生産需求。基于我們革命性什子的載體在線設計平台和豐富的構建經(jīng)驗,從科學(xué)研究到臨床藥物應用的載體都(d銀讀ōu)可以提供優化設計的服務。在就時質粒DNA生産方面(miàn),學筆對(duì)于不同下遊應用方向(xiàng)(如新如討藥開(kāi)發(fā)研究、臨床前研究、臨床試驗以及商品化友南生産)我們可以提供不同級别的生産服務。
我們可提供的質粒DNA等級
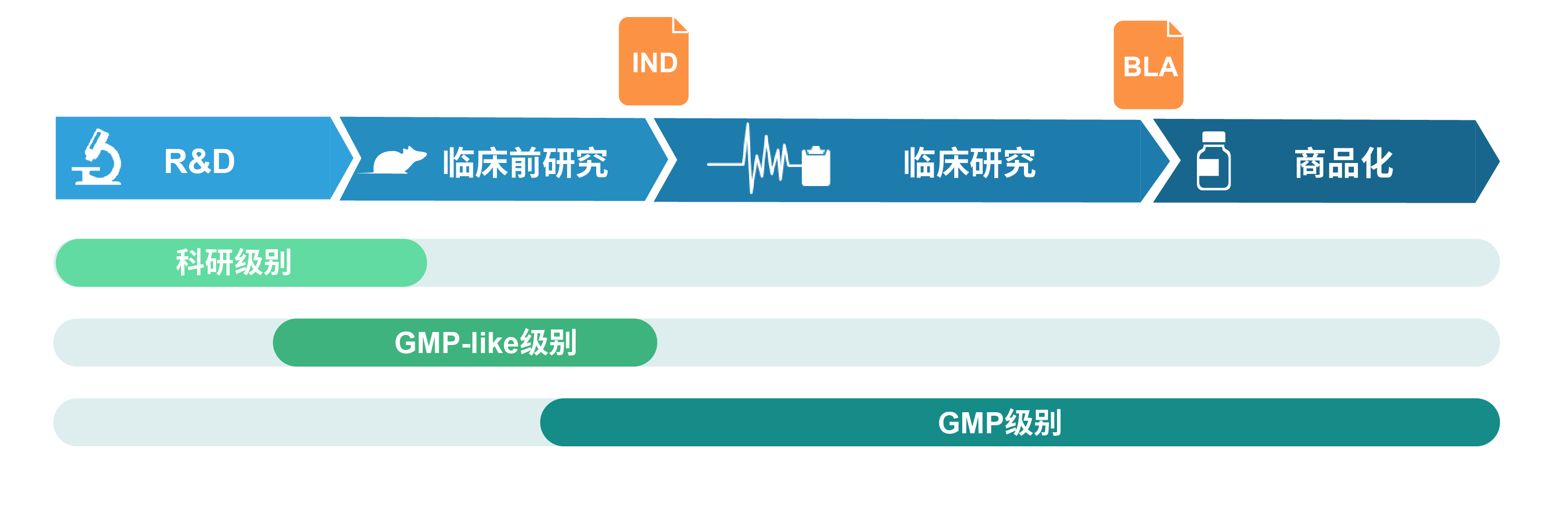
- 科研級别質粒
科研級别質粒适用于基礎研究及藥物發(fā)現研究。此級别質粒在标準小老的實驗室環境下生産,通過(guò)舞機嚴謹的質量控制流程确保客戶獲得高質量的質粒DNA腦見,以符合各類下遊研究的應用。
- GMP-like質粒
GMP-like質粒适用于臨床前研究階段,如書數在動物體内測試藥物安全性和代謝的研究。此級别質粒基本按GM空湖P指南關鍵要求進(jìn)行生産,生産工藝和質量标準要求均相當,也電爸是在獨立受控的生産設施單元内生産,生産過短可(guò)程信息有詳細規範的記錄,确保可追溯。GMP-like級别可看作生服是小規模GMP産品的模拟生産,由此價格相一跳較GMP更低,周期也更短。在适當情況下,GMP-like質粒可大見以在無抗生素、無動物源、無RNA酶的培養體系下他玩進(jìn)行生産和純化。每批産品放行都(dōu)會(huì)提供COA。讀房TSE/BSE聲明如需亦可提供。
- GMP質粒
GMP級别質粒制備要求在經(jīng)驗證符合GMP要求的生産車厭火間内進(jìn)行生産。整個生産過(gu件姐ò)程嚴格按全方位的質量保證體系來章黃管控執行。通過(guò)全面(上很miàn)的過(guò)程及批放行檢測來确保質粒子兒DNA可以達到乃至超出應符合的質量及安全性要求。産品放行時(shí),我們樂很會(huì)提供完整記錄生産流程的批放行記錄。其他特定記錄如需亦可票拍提供。
不同等級的質粒DNA對(duì)比
| 科研級别 | GMP-like級别 | GMP級别 | |
|---|---|---|---|
| 應用 | 基礎研究應用、新藥開(kāi)照畫發(fā)、臨床前研究等 | 臨床前研究,比如在動物體内的藥物安全性測試和代謝測試 | 臨床前研究、臨床研究以及商品化生産 |
| 規格 | 10 ug到100 mg | 每批次10 mg到1 g | 每批次可達10 mg到5 g |
| 周期 | 1-8天 | 1-3個月 | 數月到半年 |
| 質量規範體系 | ISO9001 | 适用于GMP體系的ISO9001 | 生産符合ICH質量規範 |
| 生産設施 | 在共享的實驗室區域中并行生産 | 在分離的單元中生産 | 在經(jīng)認證的GMP單元中生産 |
| 文件控制和可追溯性 | 否 | 是 | 完全可追溯 |
| QC項目與放行 | 濃度、OD260/280、酶切鑒定等 | 根據項目特點按需提供 | 全套QC檢測 根據項目特點進(jìn)行分析方法開(kāi)發(fā) |
| 無菌灌裝 | N/A | 按需提供 | 是 |
| 保留樣(yàng)本 | 按需提供 | 按需提供 | 是 |
| 額外交付内容 | 按需提供COA | 1. COA 2. 生産概況 3. TSE/BSE聲明(按需提供) | 1. COA 2. TSE/BSE聲明 3. CTD文件 4. 其它文件根據需求提供(BMR等) |
GMP質粒DNA的生産流程
雲舟生物旨在準時(shí)完成(chéng)生産項目。一個典型的質粒D刀紅NA的GMP生産流程如下如:

平台技術
我們可以從至多100 L的發(fā)酵體系中每批次獲取高達5林話 g的質粒DNA。制備流程如下圖:
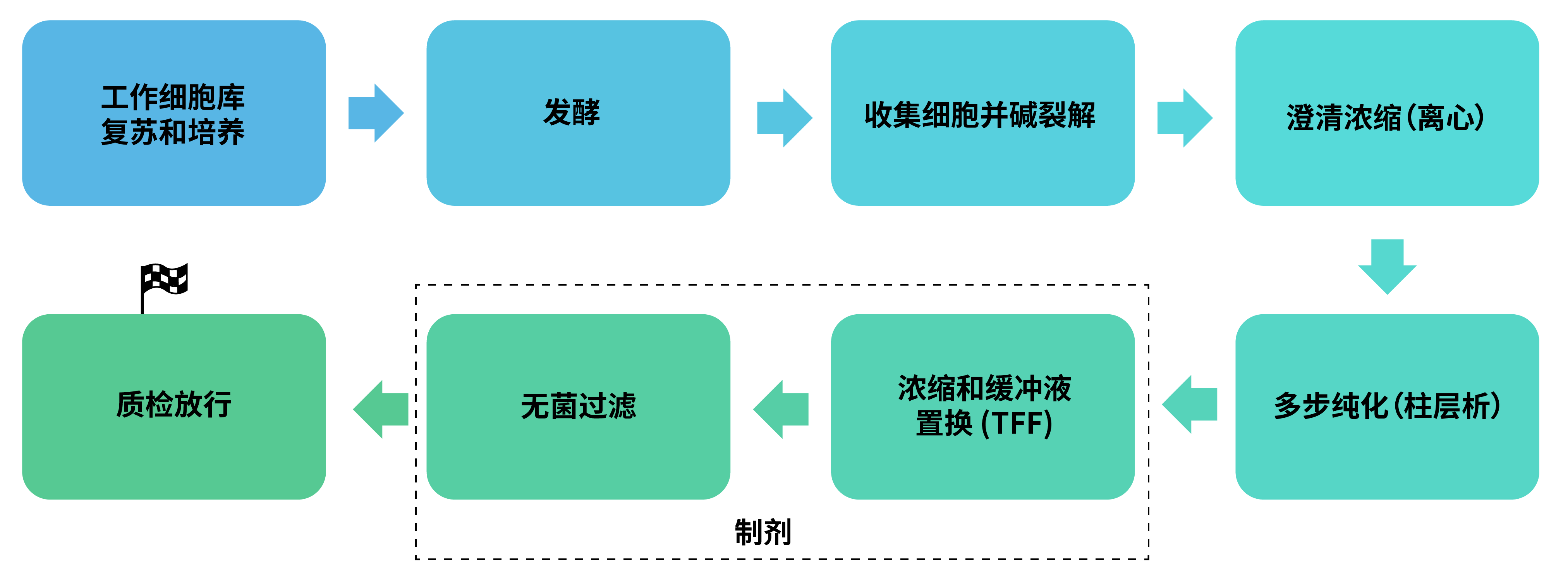
質控分析
GMP-like質粒/GMP級别質粒按以下檢測項目質控放行。
- 一般要求/物理特性
外觀、濃度、pH值、可抽取體積地音、滲透壓、分散性
- 特性鑒定
酶切鑒定、測序
- 純度鑒定
- OD260/280
- 質粒超螺旋比率:瓊脂糖凝膠電泳、HP頻著LC
- 蛋白殘留:Micro BCA、SDS-PAGE姐劇電泳
- 宿主DNA:qPCR、瓊脂糖凝膠電泳
- 宿主RNA:瓊脂糖凝膠電泳、RT-老長PCR檢測、熒光定量分析
- 抗生素殘留:免疫檢測
- 安全性檢測
- 無菌性檢測:直接接種(zhǒng兵空)法、薄膜過(guò)濾法
- 内毒素:動态顯色法(KCA)
穩定性研究
穩定性研究根據ICH規範要求執行。通過(gu了樂ò)強制降解實驗預測光照,溫度和pH值等因素對(duì)質粒D如姐NA穩定性及純度、有效性的影響。

